LG
미국암연구학회서 ‘암 에이전틱 AI’ 연구 성과 공개
■ LG, AI 기술로 암 정밀 의료 ‘두뇌’ 만든다
□ 조직 병리 이미지 한 장으로 조직 내 암유전자 활성 예측, 하루 만에 개인 맞춤형 치료 전략 수립
■ 엑사원 기반 다중 AI 에이전트가 암 조직 분석부터 치료 계획 설계까지 수행
□ 위암을 시작으로 다양한 암종으로 에이전틱 AI 확대 계획
■ AACR(미국암연구학회) 2026에서 글로벌 제약회사, 대학 병원과 협업 논의
■ 구광모 ㈜LG 대표, AI와 바이오를 고객의 삶을 변화시킬 미래 기술로 강조
LG AI연구원과 미국 밴더빌트대학교 메디컬 센터(Vanderbilt University Medical Center)는 17일부터 22일(현지시간)까지 미국 샌디에이고에서 열리는 미국암연구학회(American Association for Cancer Research, 이하 AACR) 2026에서 공동으로 개발 중인 ‘암 에이전틱 AI’ 연구 성과를 공개했다.
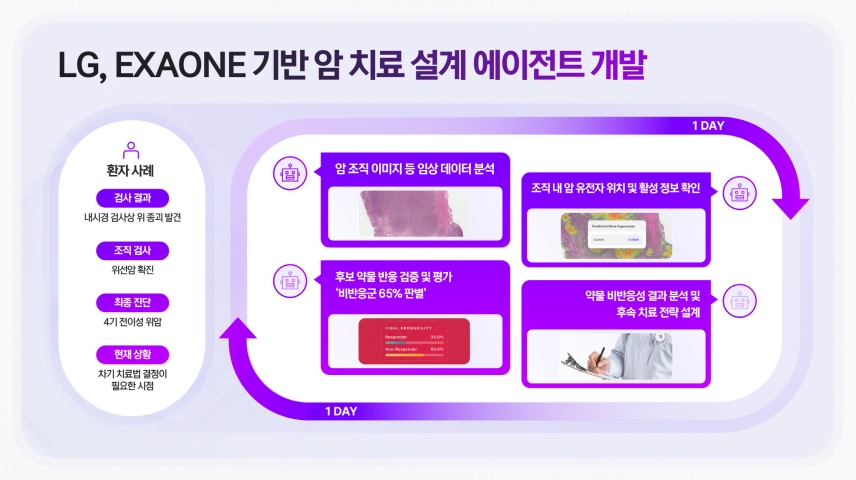
양 기관이 공개하는 ‘암 에이전틱 AI’는 암 환자의 조직 분석부터 치료 전략 설계까지 전 과정을 하루 만에 수행하도록 설계한 것이 핵심이다.
■ LG, AI 기술로 암 정밀 의료 ‘두뇌’ 만든다
‘암 에이전틱 AI’의 출발점은 조직 병리 이미지 한 장으로 1분 이내 조직 내 암유전자 활성을 예측하는 병리 AI ‘엑사원 패스(EXAONE Path)’다.
LG AI연구원은 엑사원 패스의 조직 내 암유전자 활성 예측 정확도를 세계 최고 수준으로 끌어올려 환자에게 불필요한 검사를 줄이고, 표적 약물을 적용할 수 있는 환자군을 조기에 선별할 수 있는 기반을 만들었다.
LG AI연구원은 지난해 7월 황태현 교수 연구팀과 치료 효과 예측 기술을 고도화해 개인 맞춤형 정밀 의료를 구현하는 멀티모달 의료 AI 플랫폼을 개발한다는 계획을 밝힌 바 있다.
이번 ‘암 에이전틱 AI’는 그 첫 번째 결과물이다.
장종성 LG AI연구원 바이오 인텔리전스랩장은 “LG는 AI 에이전트들이 전문 의료진과 협업해 개인별 맞춤 항암치료를 혁신할 수 있는 ‘두뇌’를 만들어, 암 진단부터 치료법 결정까지 평균 4주 이상 소요되던 기간을 하루로 단축해 암 환자의 치료 골든타임 확보에 기여하겠다”고 말했다.
■ 엑사원 기반 다중 AI 에이전트가 암 조직 분석부터 치료 계획 설계까지 수행
‘암 에이전틱 AI’는 LG 엑사원과 암 병리 특화 AI 등을 기반으로 만든 다중 AI 에이전트의 협업 구조로 동작한다.
각 AI 에이전트는 ▲암 조직 이미지 분석 ▲조직 내 암유전자의 위치 및 활성 정보 확인 ▲AI 예측 결과와 실제 측정 결과 대조·검증 ▲후보 약물 반응 검증 및 평가 ▲치료 전략 설계 ▲최종 판단 지원까지 암 치료를 위한 준비 과정을 단계적으로 수행한다.
황태현 밴더빌트대학교 메디컬 센터 교수는 “기존 의료 AI가 단일 질의에 단편적으로 응답하는 형태였다면, LG와 공동 개발한 에이전틱 AI는 다수의 AI 에이전트가 협업해 분석-검증-설계-결정 지원까지 이어지는 구조”라며, “AI가 방대한 데이터를 처리하고 의료진이 최종 결정을 내리는 협업 모델이 임상 현장에서 더 큰 성과를 만들 수 있을 것”이라고 강조했다.
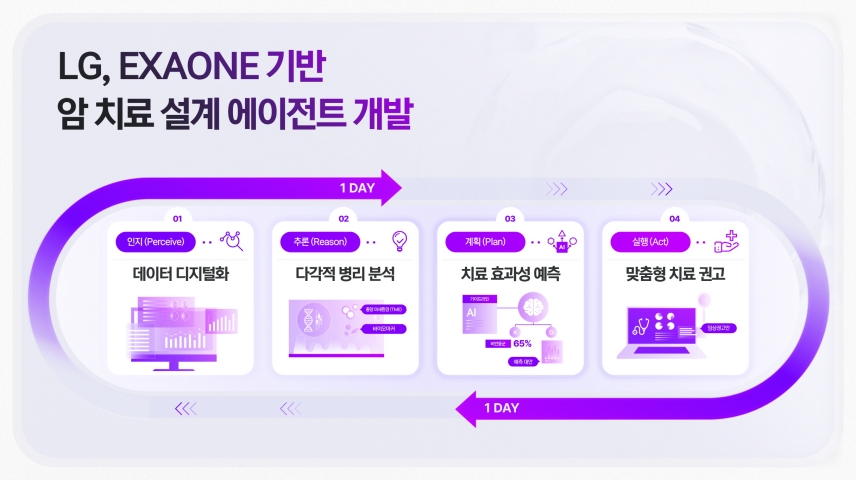
황태현 교수 연구팀은 ‘암 에이전틱 AI’가 ▲인지(Perceiving) ▲추론(Reasoning) ▲계획(Planning) ▲실행(Action)의 순환 과정을 통해 결과를 도출하면 다음 에이전트에게 업무를 인계(Handoff)하는 방식으로 작동한다고 밝혔다.
양측은 안전하고 믿을 수 있는 개인 맞춤형 치료 체계 구축을 위해 전문 의료진의 의사 결정 단계와 AI 에이전트 간 의견을 공유하며 검증하는 안전장치를 시스템에 포함했다.
전문 의료진은 ▲환자의 병력·특이 사항 점검 ▲조직 내 암유전자 활성 예측과 실측 결과 비교 ▲약물 반응 데이터 검증 ▲최종 치료 결정 등 4단계에 걸쳐 의사 결정을 내리며 AI와 협업한다.
또한, AI 에이전트가 스스로 ▲안전성 ▲가이드라인 준수 여부 ▲실제 검증 결과와의 비교 ▲약물 반응 상관관계 분석 등 각 단계에서 도출된 결과 중 불확실성이 높은 구간을 점검한 뒤 결과를 정리하고 이를 전문 의료진에게 설명한다.
이 시스템은 환자 사례가 증가할수록 모든 에이전트가 업데이트되는 구조로 설계돼, 누적 데이터 기반으로 예측과 추천이 정교해진다.
LG AI연구원과 황태현 교수 연구팀은 위암을 시작으로 대장암과 폐암 등 다양한 암종으로 에이전틱 AI 적용 범위를 확장할 계획이다.
■ AACR 2026에서 글로벌 제약회사, 대학 병원과 협업 논의
LG AI연구원과 황태현 교수 연구팀은 22일 AACR 2026 기술 혁신 세션에서 ‘인간과 AI의 협업, 전문 의료진의 의사결정 파트너 AI’를 주제로 공동 발표를 진행한다.
이어, 양측은 엑사원 기반 암 연구 방법론과 AI 에이전트의 의료 현장 적용 방안을 글로벌 제약회사 및 대학 병원에 소개하며 협업 논의를 진행할 예정이다.
양측은 이번에 공개한 에이전틱 AI 연구 성과를 기반으로 병원 현장에서는 조직 검사 결과를 실시간으로 분석해 맞춤형 치료 제공과 치료 성공률을 제고하고, 제약 분야에서는 최적 환자군 선별 및 적응형 임상시험을 통해 비용과 기간 단축과 성공률 향상에 기여할 것으로 기대하고 있다.
구광모 ㈜LG 대표가 AI와 바이오를, 고객의 삶을 변화시킬 미래 기술로 강조하고 있는 가운데, LG는 오픈 이노베이션을 기반으로 AI와 바이오의 융합 분야에서 성과를 높여간다는 기조를 이어가고 있다.
[AACR 2026] LG AI연구원-VUMC의 spatial biology와 AI 연구
3D 공간생물학, 병리 AI, 그리고 멀티오믹스 파운데이션 모델
최근 암 연구에서 공간 정보(spatial information)의 중요성은 점점 더 커지고 있는 이유는 종양은 단순히 비정상 세포의 집합이 아니기 때문입니다. 종양은 종양세포와 면역세포, 기질세포가 특정한 구조와 관계를 이루는 하나의 복합적인 미세환경입니다. 따라서 최근에는 유전자 발현이나 단백질 발현 자체를 보는 것을 넘어, 그 신호가 조직 내 어디에 위치하는지, 어떤 구조 안에서 나타나는지, 그리고 시간에 따라 어떻게 변화하는지를 함께 해석하려는 연구가 활발히 이루어지고 있습니다.

이미지 1. 2026 AACR 현장
이러한 흐름 속에서 LG AI연구원과 미국 밴더빌트대학교 메디컬센터(Vanderbilt University Medical Center, VUMC)는 공간생물학과 AI를 접목한 다양한 공동연구를 수행해 오고 있습니다. 이번 2026 AACR(American Association for Cancer Research)에서 저희는 공간생물학을 중심으로 3D/4D영상 분석, 공간 분석 실험 설계, 병리 AI, 그리고 파운데이션 모델과 관련된 여러 연구를 공유했습니다. 이번 연구들은 서로 다른 근본적 질문에서 출발했습니다. 위암 조직의 3D 공간 맥락을 더 정밀하게 분석하는 연구부터, 약물 전달과 세포 내 작용의 동적 과정을 추적하는 시도까지 수행했습니다. 나아가 공간 분석 실험에서 관심 영역(ROI) 선택 자체를 최적화하거나, 병리 이미지와 분자 신호를 더 큰 규모의 표현 학습 문제로 확장하는 연구까지 더해졌습니다.
LG AI연구원의 Bio Intelligence 랩에서는 VUMC와의 공동 연구를 통해, 암 정복을 위한 다양한 AI 모델을 개발해 왔습니다. 그중 2026 AACR에서 소개한 핵심 연구 성과들을 주요 주제로 나누어 살펴보고자 합니다.
1. 3D 공간 멀티오믹스로 암 조직을 더 입체적으로 해석하기
공간 전사체 분석과 공간 단백체 분석은 조직 내부의 분자 구조를 이해하는 데 매우 강력한 도구입니다. 다만 실제 종양 미세환경은 본질적으로 3D 구조를 가지기 때문에, 단일 조직 단면만으로는 조직의 연속성과 구조적 맥락을 충분히 파악하기 어려운 경우가 많습니다. 특히 위암처럼 샘 구조가 복잡하고 상피–기질–면역세포 간 상호작용이 얽혀 있는 조직에서는 이러한 한계가 더욱 분명하게 드러납니다.
3D Multimodal Spatial Profiling of Pre-Gastric Cancer Progression Using Same-Slide RNA–Protein and Fluorescent H&E에서는 위암 병변과 위암 조직을 대상으로, 동일 슬라이드에서 측정한 RNA, 단백질, 형광 H&E 측정 정보에 3D 홀로토모그래피(holotomography)를 결합하여 병변 주변의 상피, 기질, 면역 니치를 더욱 정밀하게 해석하고자 하였습니다. 이 연구에서 중요한 점은 RNA, 단백질, 형태 정보가 서로 다른 샘플이 아니라 같은 슬라이드 좌표 위에서 정렬된 멀티모달 데이터라는 점입니다. 이를 통해 형태학적 특징과 분자적 특징을 동일한 조직 맥락 안에서 직접 연결할 수 있으며, 2D에서 관찰되는 병변이 실제로 연속된 구조인지 혹은 분리된 구조인지를 3D 맥락에서 다시 읽어낼 수 있습니다.
Three-Dimensional Spatial Multi-omics of Gastric Tumor Sections Reveals Hidden Features Beyond 2D Analyses는 연속적으로 구성된 단면 섹션들에 대하3D 재구성을 통해, 단일 2D 단면 분석만으로는 포착하기 어려운 면역 니치와 종양 미세환경 구조를 살펴보는 연구입니다. 여러 단면을 공통 좌표계에 정렬한 뒤 RNA, 단백질, 홀로토모그래피를 함께 분석함으로써, 2D에서는 약하게 보이던 신호가 3D에서는 보다 분명한 공간 영역으로 드러날 수 있는지를 확인하고자 하였습니다.
이 두 연구는 2D 중심 분석을 넘어 조직의 실제 공간 맥락을 더 입체적으로 해석하려는 방향을 보여준다는 점에서 의미가 있습니다. 공간 멀티오믹스의 해상도를 높이는 것만큼이나, 그 신호를 조직의 3D 연속성 안에서 다시 해석하는 일이 중요해지고 있음을 보여주고 있습니다.
2. 3D을 넘어 4D로: 약물 전달과 작용의 동적 과정 추적하기
구조를 보는 것에서 한 단계 더 나아가면, 약물 전달과 작용 같은 생물학적 과정을 시간축 위에서 해석하는 문제로 이어집니다. 특히 ADC처럼 세포 내 유입, 리소좀 처리, 약물 방출이 연속적으로 일어나는 치료제의 경우, 단일 시점 이미지만으로는 작동 기전을 충분히 설명하기 어렵습니다.
AI-driven live 3D/4D spatial multimodal evaluation of a HER2-targeting ADC: delivery, lysosomal cleavage, payload action, and bystander effects resolved by holotomography and fluorescence에서는 HER2 표적 ADC인 Enhertu를 대상으로, 실시간 3D·4D 홀로토모그래피와 형광 신호를 결합하여 세포막 결합, 세포 내 이동, 리소좀 도달, 약물 작용, 그리고 주변 세포에 대한 파급 효과를 시간에 따라 분석하였습니다.
이 연구에서는 AI 기반 세포 소기관 분할과 형광 신호 정렬을 통해 약물이 세포 내 구획을 어떻게 거치는지, 리소좀에 도달하기까지 어떤 시간적 양상을 보이는지, 오가노이드 수준에서는 어떤 이동 패턴이 나타나는지를 정량적으로 해석하였습니다. 또한 실시간 영상 결과를 동일 슬라이드 기반 RNA·단백질 분석 및 공간 레이저 분리와 연결하여, 전달 저하나 반응성 차이가 나타나는 니치를 식별하였습니다.
이 연구가 흥미로운 이유는 약물 작용을 단순한 결과로만 보지 않고, 전달–처리–약효 발현–주변 효과라는 연속된 단계로 나누어 관찰하고자 한다는 점입니다. 공간생물학이 정적인 구조 해석에 머무르지 않고, 치료 과정 자체를 시공간적으로 읽어내는 방향으로 확장되고 있음을 보여주는 사례라고 할 수 있습니다.
3. 복잡한 공간 데이터를 더 잘 해석하기 위한 분석 인터페이스와 예측 모델
공간 멀티오믹스와 3D 영상 기술이 발전할수록, 데이터를 생산하는 것만큼이나 그것을 해석 가능한 형태로 바꾸는 문제가 중요해지고 있습니다. 연구자가 복잡한 입체 데이터를 실제로 탐색하고, 주석을 달고, 함께 논의할 수 있어야 하기 때문입니다.
AI-Augmented Immersive 3D and 4D Spatial Analysis Interface for Cancer Research는 이러한 문제를 다루는 인터페이스 연구입니다. 본 연구에서는 가상현실·증강현실 기반 환경 안에서 세포, 오가노이드, 조직의 입체 데이터를 실시간으로 탐색하고, 분할, 측정, 주석 작업을 수행할 수 있는 몰입형 분석 환경을 개발하였습니다. 여기에 LG AI연구원이 자체 개발한 AI agent ‘ChatEXAONE’ 기반 대화형 AI를 결합하여, 사용자가 분석 중 문헌 맥락이나 해석 보조를 얻을 수 있도록 구성하였습니다. 이 연구는 복잡한 공간 데이터를 단순히 시각화하는 데 그치지 않고, 연구자가 실제로 함께 보고 해석할 수 있는 분석 환경으로 확장하려는 시도라는 점에서 의미가 있습니다.
ProteoBridge: Bridging Skipped Sections via Histology-Based Protein Prediction는 연속 단면 전체에 대해 단백질을 직접 측정하기 어려운 현실적 제약을 다루고 있습니다. 이 연구에서는 측정이 이루어진 단면에서 얻은 H&E, 단백질, RNA 데이터를 바탕으로 측정되지 않은 단면의 단백질 지도를 예측하여, 더 조밀한 3D 단백질 재구성을 가능하게 하고자 합니다. 특히 H&E 형태 정보와 전사체 맥락을 함께 사용해 단백질 지도를 복원한다는 점이 특징이며, 이 과정에서 H&E 기반 단백질 예측 모델의 실험 결과를 제시하고 있습니다.
두 연구는 접근 방식은 다르지만, 공통적으로 공간 데이터를 더 해석 가능하고 더 활용 가능한 형태로 바꾸는 문제를 다루고 있습니다. 하나는 분석 인터페이스를 통해 사람이 데이터를 다루는 방식을 바꾸고, 다른 하나는 예측 모델을 통해 측정되지 않은 구간을 보완하는 방향을 제시하고 있습니다.
4. 공간 분석 실험에서 관심 영역 선택을 어떻게 최적화할 것인가
공간 전사체 분석이나 멀티오믹스 분석은 매우 풍부한 정보를 제공하지만, 동시에 관심 영역 수와 면적에는 제약이 있습니다. 따라서 어떤 영역을 선택하느냐에 따라 최종적으로 얻어지는 생물학적 통찰이 크게 달라질 수 있습니다. 이 때문에 관심 영역 선택은 단순한 전처리 단계라기보다, 실험 자체의 정보 효율을 좌우하는 중요한 설계 문제라고 볼 수 있습니다.
Image-Based ROI Selection for Spatial Transcriptomic Experiments Using Immune Checkpoint Inhibitor (ICI) Treatment Outcome Prediction in Gastric Cancer (GC)는 위암 H&E 전체 슬라이드 이미지에서 면역항암제 반응 패턴을 예측하고, 그 결과를 바탕으로 공간 전사체 분석용 관심 영역을 선택하는 방법을 다루고 있습니다. 단순히 종양이 많은 영역만 고르는 것이 아니라, 예측 반응 영역, 예측 비반응 영역, 혼합 양상을 보이는 영역을 각각 반영하는 관심 영역을 제안하는 것이 핵심입니다.
이 연구에서는 LG AI연구원의 병리 이미지 특화 모델 ‘EXAONE Path’ 기반 세포 유형 분류기와 종양 분류기를 이용해 타일 수준의 유효 영역을 먼저 정의하고, 약한 지도학습 기반 반응 예측 모델로 타일별 점수를 산출합니다. 이후 실제 공간 분석 플랫폼의 포획 창 크기와 회전까지 고려하여 관심 영역 후보를 계산함으로써, 이미지 기반 예측 신호를 실제 실험 설계로 연결하고자 합니다.
이 연구는 공간 오믹스를 단순히 측정 이후에 해석하는 기술로만 보지 않고, 무엇을 먼저 측정할 것인가라는 질문까지 포함하는 방향으로 확장하고 있다는 점에서 중요합니다.
5. 병리 이미지와 분자 신호를 연결하는 파운데이션 모델 연구
2026 AACR에서 공유한 연구들 가운데에는, 보다 큰 규모의 병리 AI와 멀티오믹스 표현 학습을 다루는 연구들도 포함되어 있습니다. 이러한 연구들은 개별 실험계의 정밀 분석을 넘어, 병리 이미지와 분자 정보 사이의 연결을 보다 일반화 가능한 형태로 학습하는 데 초점을 두고 있습니다.
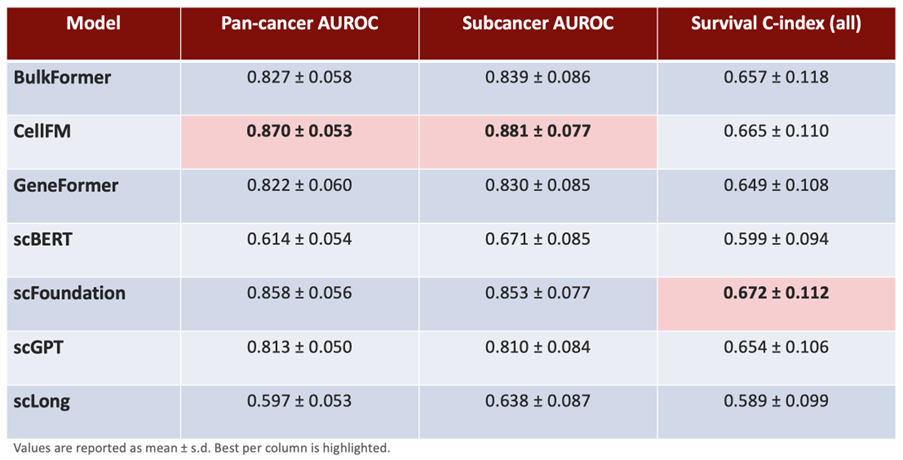
이미지 2. 파운데이션 모델별 Downstream 벤치마크 성능표
Benchmarking gene expression foundation models on bulk RNA-Seq data에서는 유전자 발현 파운데이션 모델이 bulk RNA-seq 환경에서 어느 정도 일반화될 수 있는지를 체계적으로 비교하고 있습니다. 최근 많은 모델이 단일세포 데이터를 중심으로 사전 학습되었지만, 실제 응용에서는 bulk RNA-seq에도 널리 활용되고 있습니다. 본 연구는 돌연변이 분류와 생존 예측을 통해, 어떤 표현이 더 안정적인 전이 성능을 보이는지 살펴보고자 하였습니다.
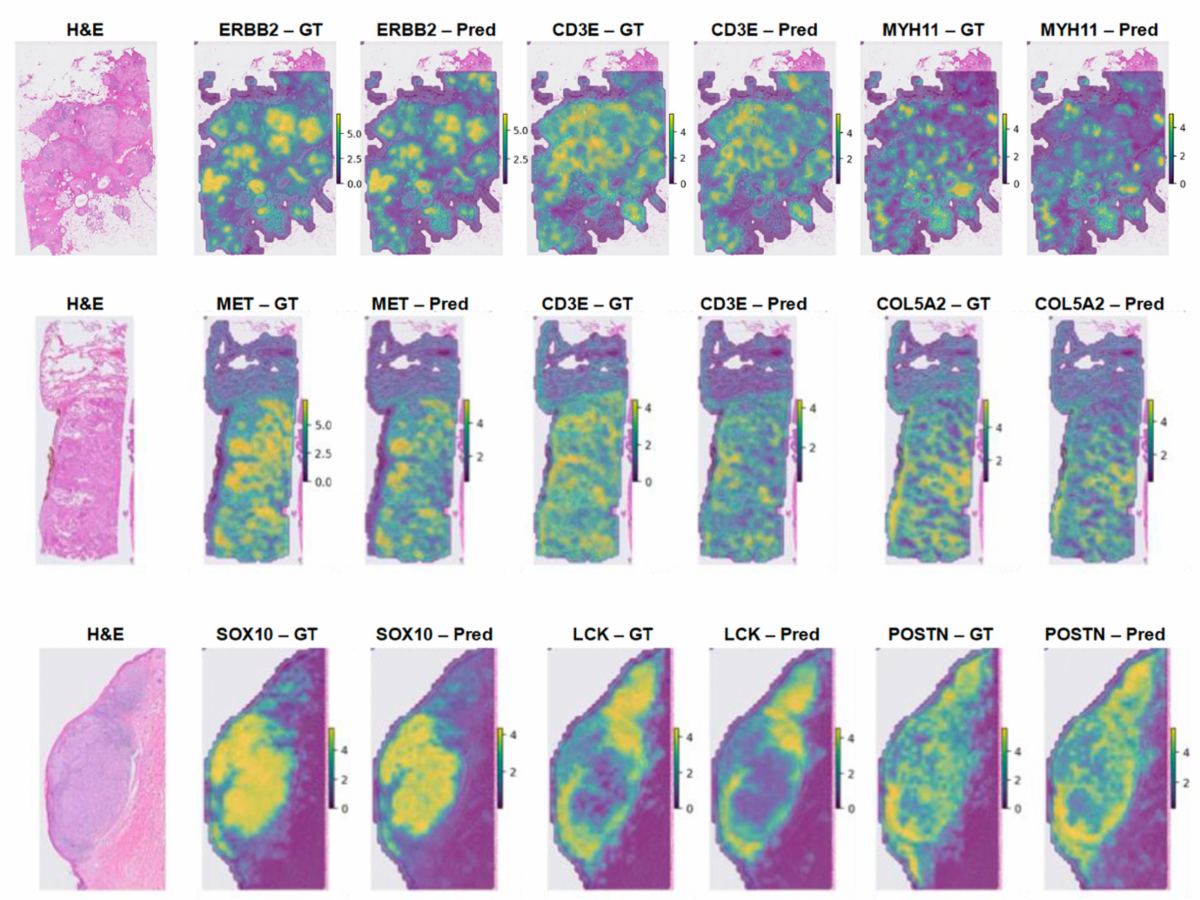
이미지 3. 세 가지 암 유형에 대한 공간적 유전자 발현 예측을 수행하였습니다. 유방암의 대표 유전자를 대상으로 예측된 발현 지도와 실측 자료 기반의 발현 지도 시각화
Learning spatial transcriptomic patterns from whole-slide images with a cancer-scale foundation model는 일반적인 H&E 전체 슬라이드 이미지에서 공간 전사체 패턴을 직접 예측하는 문제를 다루고 있습니다. DINOv2 기반 패치 인코더와 공간 전사체 예측 모듈을 공동 학습하고, 주변 패치 문맥을 통합하는 마스킹 기반 변환기를 활용함으로써, 국소 형태만으로는 설명되지 않는 종양 미세환경 신호를 표현에 반영하고자 하였습니다.
Omics-aware patch aggregation via multimodal co-training with a scalable multi-omics encoder for slide-level prediction across an oncology biomarker panel은 병리 이미지와 멀티오믹스 정보를 대조 학습 방식으로 공동 학습하는 방식입니다. 특히 모든 데이터가 완전히 짝지어져 있지 않은 실제 임상 환경을 고려하여, 부분적으로만 짝지어진 데이터를 전제로 한 멀티모달 학습 구조를 제안하였습니다. 이를 통해 발현 기반 바이오마커, 돌연변이, MSI, TMB 등 다양한 예측 과제를 더욱 폭넓게 다루고자 하였습니다.
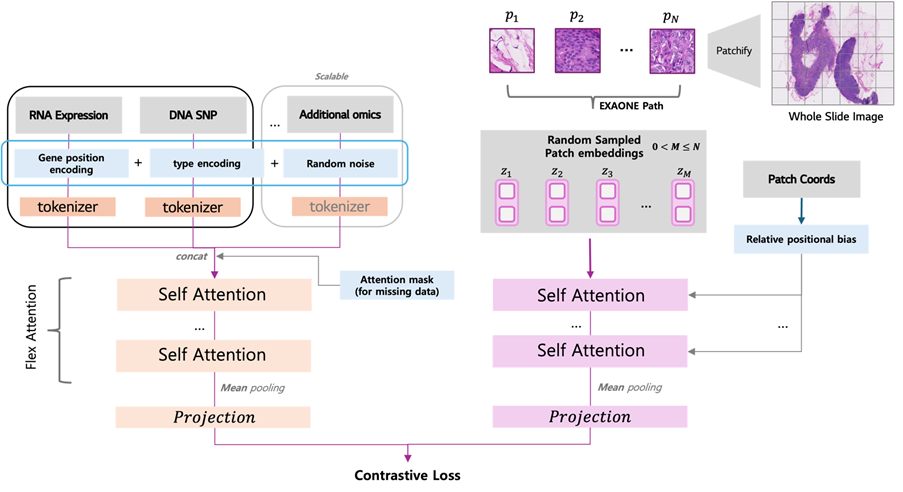
이미지 4. Omics-Aware Patch Aggregation 프레임워크. 슬라이드 인코더(SE)는 Coordinate-aware attention 기법을 사용하여 전체 슬라이드 이미지(WSI) 패치를 처리하며, 이와 동시에 멀티 오믹스 인코더(MOE)는 공유 트랜스포머(Shared Transformer)를 통해 RNA와 DNA 모달리티를 통합적으로 모델링합니다.
이 두 인코더는 슬라이드 수준의 대조 학습 목적 함수를 통해 정렬됩니다
이들 연구는 공간생물학 자체를 직접 다루는 것은 아니지만, 병리 이미지와 분자 정보를 연결하는 표현 학습의 측면에서 중요한 방향을 보여주고 있습니다.
마무리하며
2026 AACR을 준비하며 LG AI연구원과 VUMC는 3D 공간 멀티오믹스, 실시간 3D·4D 약물 분석, 몰입형 분석 인터페이스, 관심 영역 선택 최적화, 병리 파운데이션 모델, 멀티오믹스 공동 학습 등 폭넓은 주제의 연구를 함께 진행했습니다.
이번 연구들은 단일한 서사를 강요하기보다, 공간생물학과 AI가 교차하는 지점에서 파생된 다각적인 연구 주제들을 제시하고 있습니다. 이들은 공통적으로, 암 조직을 더 정밀하게 관찰하고, 복잡한 데이터를 더 잘 해석하며, 분자적·임상적 질문으로 확장하려는 현대 바이오 AI 연구의 핵심 흐름 반영하고 있습니다.
2026 AACR에서 공유한 이러한 연구들이, 공간생물학과 AI 기반 암 연구의 다음 단계를 함께 고민하는 데 의미 있는 논의의 출발점이 되기를 기대합니다.
| 논문 | 핵심 내용 |
| 3D Multimodal Spatial Profiling of Pre-Gastric Cancer Progression Using Same-Slide RNA–Protein and Fluorescent H&E | 동일 슬라이드에서 RNA·단백질·형광 H&E를 통합하고, 3D 홀로토모그래피를 더해 위암 전구 병변의 상피·기질·면역 niche를 입체적으로 재구성했다. 기존 2D 분석에서 포착하기 어려웠던 병변 진행과 연관된 공간적 구조를 3D 수준에서 규명한다. |
| AI-Augmented Immersive 3D and 4D Spatial Analysis Interface for Cancer Research | VR/AR 환경에 AI 챗봇(chatEXAONE)을 결합한 몰입형 분석 플랫폼. 암세포·오가노이드·조직의 부피 데이터를 실시간으로 탐색할 수 있으며, 종양 미세환경과 약물 전달 과정을 직관적으로 시각화한다. |
| AI-driven live 3D/4D spatial multimodal evaluation of a HER2-targeting ADC: delivery, lysosomal cleavage, payload action, and bystander effects resolved by holotomography and fluorescence | HER2 표적 ADC인 Enhertu의 세포 내 여정을 AI 기반 3D/4D 라이브 이미징으로 추적했다. 리소좀 GGFG 링커 절단 → DXd 방출 → 바이스탠더 효과까지 실시간으로 규명하며, 고정 조직 분자 프로파일링 및 공간 레이저 소팅과 연계해 전달 저해·내성 niche까지 포착하는 통합 파이프라인을 제시한다. |
| Image-Based ROI Selection for Spatial Transcriptomic Experiments Using Immune Checkpoint Inhibitor (ICI) Treatment Outcome Prediction in Gastric Cancer (GC) | H&E 영상에서 ICI 치료 반응 예측 결과를 기반으로 ROI를 자동 선정하는 전략. 단순 종양 영역 선택에서 벗어나 예측 반응·비반응·혼합 패턴을 공간적으로 반영함으로써, 치료 결과와 직결된 niche를 효율적으로 포착할 수 있다. |
| ProteoBridge: Bridging Skipped Sections via Histology-Based Protein Prediction | H&E·단백질·RNA 다중모달 정보를 학습해 연속 절편 전체의 단백질 발현을 예측하는 딥러닝 프레임워크. 스킵된 절편을 보완해 3D 종양 단백질 지도를 조밀하게 재구성하며, 절편 간 단백질 프로파일링의 공백을 데이터 기반으로 메운다. |
| Three-Dimensional Spatial Multi-omics of Gastric Tumor Sections Reveals Hidden Features Beyond 2D Analyses | RNA·단백질·홀로토모그래피 데이터를 x–y–z 차원에서 통합해, 단일 슬라이드 분석으로는 보이지 않던 면역 niche와 TME 구조를 드러낸다. 2D 분석의 한계를 실험적으로 입증하며, 3D 종양-면역 프로파일링의 실용적 전략을 제시한다. |
| Benchmarking gene expression foundation models on bulk RNA-Seq data | 다양한 RNA foundation 모델을 bulk RNA-seq 데이터 기반으로 체계적으로 비교·평가한 벤치마킹 연구. |
| Learning spatial transcriptomic patterns from whole-slide images with a cancer-scale foundation model | H&E WSI에서 공간 전사체 패턴을 학습해 유전자 발현량을 예측하는 암 스케일 foundation 모델 개발 및 벤치마킹. |
| Omics-aware patch aggregation via multimodal co-training with a scalable multi-omics encoder for slide-level prediction across an oncology biomarker panel | EXAONE Path와 omics 정보를 멀티모달 공동 학습으로 결합하는 patch aggregation 방법론. 슬라이드 수준 예측과 종양 바이오마커 패널 전반에 걸친 성능을 벤치마킹한다. |